ピックアップコンテンツ
- ホーム
- ピックアップコンテンツ
- <プレスリリース>【世界初】タンパク質構造決定を劇的に加速させる 「ROCKET」法を開発 AI予測と実験データを融合した革新的手法(農学部・奥村 裕紀)
タンパク質の立体構造を解明することは、生命現象の理解や新薬開発において極めて重要です。
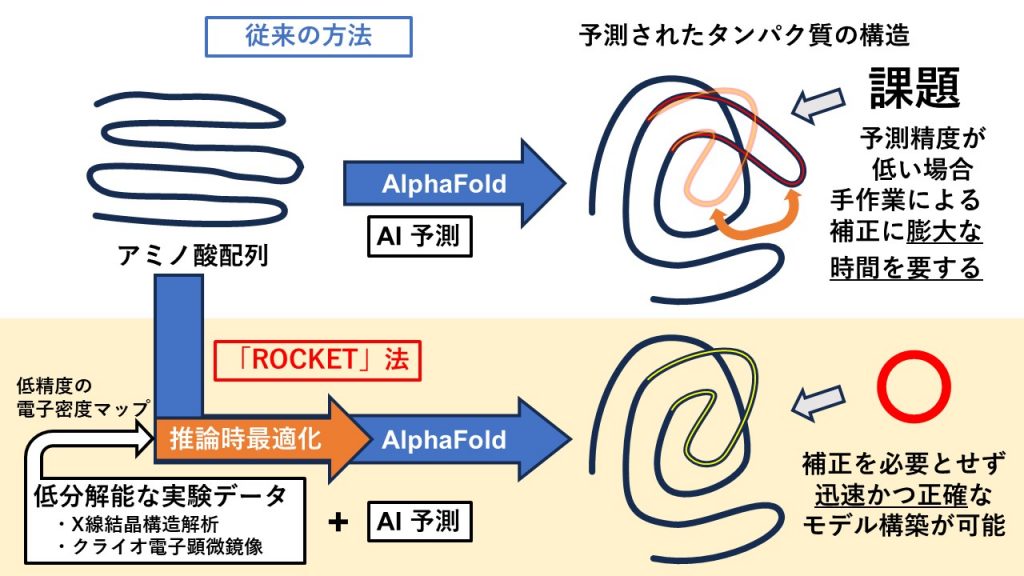
名城大学農学部の奥村裕紀教授(生物化学、分子細胞生物学)、スウェーデン・カロリンスカ研究所のLuca Jovine(ルカ・ヨヴィネ)教授、イギリス・ケンブリッジ大学のRandy J. Read(ランディ・リード)教授らの国際共同研究チームは、AIタンパク質構造予測ツール「AlphaFold」注1)を実験データの解析に直接統合する新手法「ROCKET」を開発しました。
本手法では、AIのニューラルネットワーク自体を実験データに適合(最適化)させることで、従来は手作業で行われていた補正を不要とし、高精度かつ高速な立体構造決定を可能にしました。さらに、低分解能の実験データに対しても、AIが有する事前知識(Prior / プライア)注2)を活用することで、高い信頼性を持つ分子モデルの構築が可能であることを示しました。
本技術は、構造生物学における解析プロセスの効率化と高度化を同時に実現するものであり、生命科学の基盤技術を刷新する技術として期待されます。
本研究成果は、2026年4月1日(日本時間)、英国の科学誌『Nature Methods』にオンライン掲載されました。
【ポイント】
・AIの知識を実験データ(X線結晶構造解析注3)やクライオ電子顕微鏡注4)など)の解釈プロセスに直接組み込む新技術を確立。
・タンパク質の機能・構造解析に深い知見を持つ奥村教授が共同研究に参加。AIによる予測と実際の実験データとの融合における検証に貢献。
・低分解能な実験データからでも、AIの事前知識を借りることで、極めて正確な分子モデルの構築が可能に。
掲載論文
【題 名】AlphaFold as a prior: experimental structure determination conditioned on a pretrained neural network
【著者名】Alisia Fadini,Minhuan Li,Airlie J. McCoy,Suresh Banjara,Hiroki Okumura,Eve Napier,Pietro Fontana,Amir R. Khan,Luca Jovine,Thomas C. Terwilliger,Randy J. Read,Doeke R. Hekstra,Mohammed AlQuraishi
【掲載誌】Nature Methods
【掲載日】2026年4月1日
【DOI】 https://doi.org/10.1038/s41592-026-03047-4
プレスリリース本文はこちら
https://www.meijo-u.ac.jp/news/asset/dd28f4c851a2b6869892366134892319.pdf
【用語解説】
注1)AlphaFold(アルファフォールド):
Google DeepMind社が開発した人工知能(AI)によるタンパク質構造予測ツール。アミノ酸配列の情報から、そのタンパク質がどのような立体構造をとるかを極めて高い精度で予測し、構造生物学に革命をもたらした。
注2)事前知識(Prior / プライア):
統計学や機械学習の用語で、新しいデータを見る前にあらかじめ持っている情報の量や質のこと。本研究では、AlphaFoldが膨大なタンパク質データから学んだ「タンパク質として物理的に正しい形」という知識を、実験データの解析を助ける「ガイド」として活用している。
注3)X線結晶構造解析:
タンパク質の結晶にX線を照射し、その回折パターンを解析することで原子レベルの立体構造を決定する手法。創薬や生命現象の解明において最も信頼性の高い標準的な解析法の一つ。
注4)クライオ電子顕微鏡:
生体試料を急速凍結して自然に近い状態で観察し、コンピュータ解析で原子レベルの3D構造を再現する技術。タンパク質の結晶化が不要なため、創薬や生命科学の研究を飛躍的に進化させている。
注5)電子密度マップ:
X線結晶構造解析などの実験によって得られる、タンパク質分子内の電子の分布を示した3次元の地図。研究者はこのマップの中に原子のモデルを当てはめていくことで、正確な立体構造を決定します。
注6)推論時最適化(Inference-time optimization):
AIが学習済みの知識を使って答えを出す(推論)際に、手元にある特定のデータ(今回の場合は実験データ)に最も適合するように、AI内部の数値を微調整する技術。これにより、一般的な予測を「目の前の事実」に即した形へカスタマイズできる。